

我々のグループでは、紫外~可視~赤外領域における分光実験および量子化学計算を行うことにより、分子クラスターおよびクラスターイオンの構造およびダイナミックスに関する研究を推進している。現在は、金属イオンと溶媒分子の相互作用に注目し、以下の課題に取り組んでいる。(1) 金属イオンの配位および溶媒和構造、(2) イオン–溶媒および溶媒–溶媒相互作用の協奏と競合、(3) 気相中とバルク溶液中におけるイオンの配位数の比較、(4) 溶媒和金属イオンの構造に対する温度効果、(5) 金属イオンと生体関連分子との相互作用、など
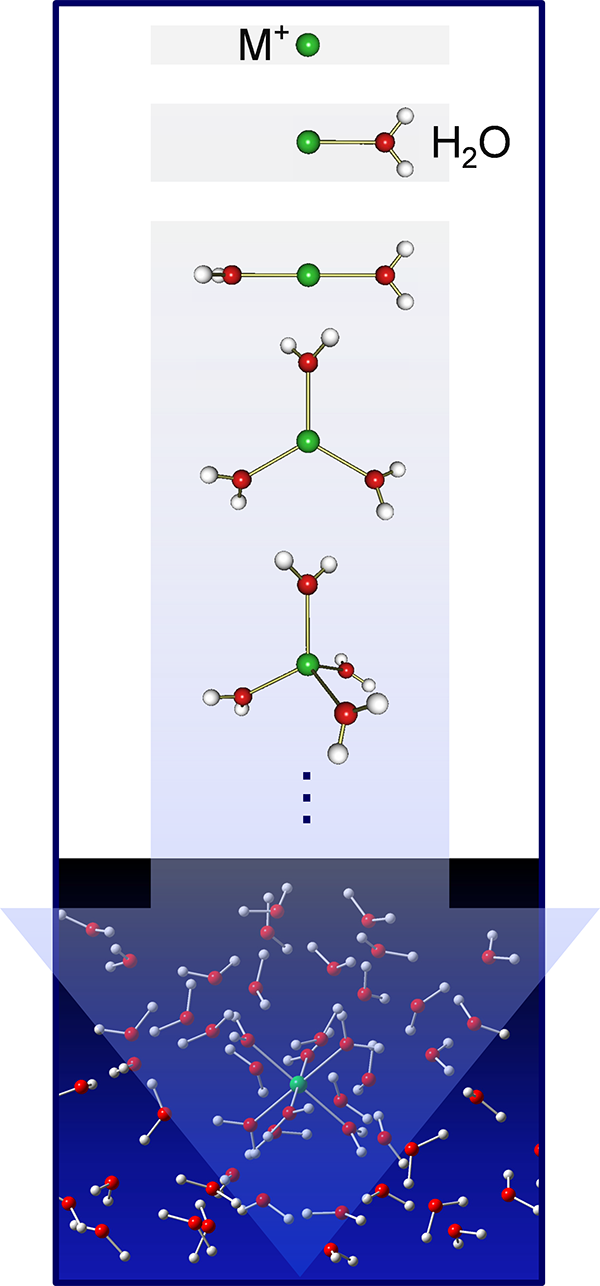
溶液中におけるイオンの性質は、化学および生物学の最も基本的な側面の1つである。特に、金属イオンの水和は、触媒作用、ホスト–ゲスト化学、金属酵素の構造と機能、細胞膜の選択的透過性などにおける金属の役割を理解する上で重要である。溶液中における金属イオンの水和構造は、様々な実験技術を使って研究されてきた。例えば、X線および中性子線回折実験により、水和金属イオンの静的構造が決定されている。しかし、配位数 (金属イオンに直接結合している水分子数) が曖昧なままの金属もある。
一方、気相中における溶媒和金属イオンは、イオンの溶媒和について分子レベルで解明するための格好の研究対象である。とりわけ赤外分光は、配位および溶媒和構造を研究するための強力な手段である。孤立した水分子の振動数は溶媒和により変化する。特に、OH基が水素結合を形成すると、そのOH結合の伸縮振動は低波数側に大きくシフトするが、水素結合とは無関係のOH結合の振動数はわずかにシフトするだけである。分子間水素結合が形成され始める水分子数を赤外分光法で調べることにより、配位数を決定することが可能である。
我々は、気相中における溶媒和金属イオンの赤外分光を行うことにより、金属イオンの配位および溶媒和構造を解明してきた。溶媒和金属イオンM+(solv)n (Mは金属原子、solvはH2O、NH3、CH3OHなどの溶媒分子) をレーザー蒸発 / 超音速ジェット法により生成する。溶媒分子数 (nの値) を特定するために質量選別を行った後、M+(solv)nのOHあるいはNH伸縮振動領域の赤外光解離スペクトルを測定する。M+(solv)nの安定構造とその赤外スペクトルを予測するために、量子化学計算を行う。これまでの成果をまとめると次のようになる。
タンパク質や酵素の多くがその活性部位に金属イオンを含んでいる。例えば、タンパク質ドメインの1つであるジンクフィンガーの構造は、亜鉛イオンが結合することにより安定化している。また、様々ながんに対する抗がん剤として使用されているシスプラチンは、白金イオンを含む薬剤である。このような系において、金属イオンと生体分子の間の相互作用が重要な役割を果たしている。我々は、金属–生体分子間相互作用をモデル化するために、金属イオンと生体関連分子からなる錯体に注目し、溶液中における分光実験により研究している。
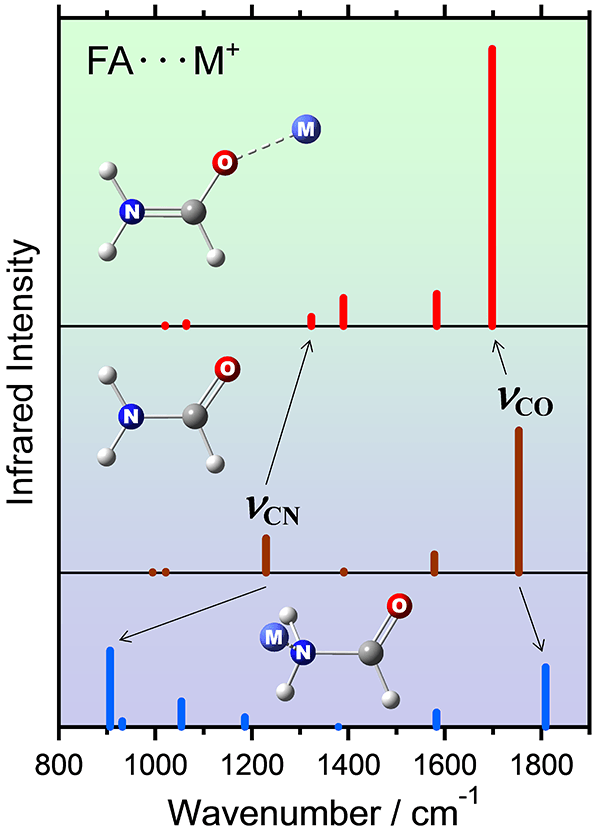
アミノ酸2分子が脱水縮合することによりペプチド結合 (–OC–NH–) が形成される。ペプチド結合は科学の様々な分野において特別な関心を集めている。ホルムアミド(FA)はペプチド結合を有する最小の分子である。FA分子が金属イオンに配位すると、COおよびCN結合の伸縮振動数 (νCOおよびνCN) がシフトする。FA分子がO原子で配位するとνCOが低波数、νCNが高波数シフトするのに対して、N原子で配位するとνCOが高波数、νCNが低波数シフトする。金属イオンのFA溶液について赤外分光を行うと、これらのシフトを観測することができる。我々の研究目的は、金属イオンとの相互作用にFA分子のどの配位部位が関与しているのかを明らかにすること、また、分光実験の結果を理論計算により定量的に解釈することである。その研究結果は、溶液中のアミノ酸やポリペプチドの立体配座構造に関する情報を引き出すのに役立つであろう。
我々は、FA純液体および一連の金属イオンのFA溶液に対して、減衰全反射赤外分光法による研究を進めている。FA分子の配位に伴う振動数シフトについての従来の考え方が必ずしも正しくないことが分かってきた。